2025年第二季的美國FDA 510(k)數據,為全球數位醫材產業的發展提供了關鍵線索。本篇分析聚焦於本季數據所揭示的市場機會與競爭現實,旨在為醫材企業、新創團隊與投資機構的策略佈局提供參考。
本篇重點 (Key Takeaways)
- 市場焦點: AI影像軟體 (QIH) 以24件許可證,成為2025年第二季最熱門的FDA 510(k)法規路徑。
- 競爭壁壘: 市場競爭的關鍵壁壘是「法規經驗」。擁有6次以上核准經驗的「專家級」玩家佔據了市場近45%的主導地位。
- 效率差距: 專家級玩家的產品平均上市時間,比較新手級玩家有近40天的顯著優勢,凸顯了經驗的量化商業價值。
本篇分析資料範圍為2025年4月1日至6月30日期間,美國FDA所核准之Class II 510(k)醫療器材許可證。
市場焦點:AI影像軟體成為主導力量
本季數據最明確的信號,來自於AI在醫學影像領域的加速滲透。
純軟體(Software as a Medical Device, SaMD)的創新能量尤其顯著,產品代碼為 QIH (Automated Radiological Image Processing Software, 自動化放射影像處理軟體) 的品項以24件的數量高居首位。這股軟體驅動的浪潮,也正深刻地改變著硬體平台的樣貌,本季同樣名列前茅的智慧平台 IYN (System, Imaging, Pulsed Doppler, Ultrasonic, 脈衝都卜勒超音波影像系統),正是「軟硬整合」趨勢的最佳體現。它們不再只是硬體,而是搭載先進演算法的智慧平台。此趨勢同步體現在臨床應用上,放射科(Radiology) 以120件許可證,成為本季最活躍的臨床部門。
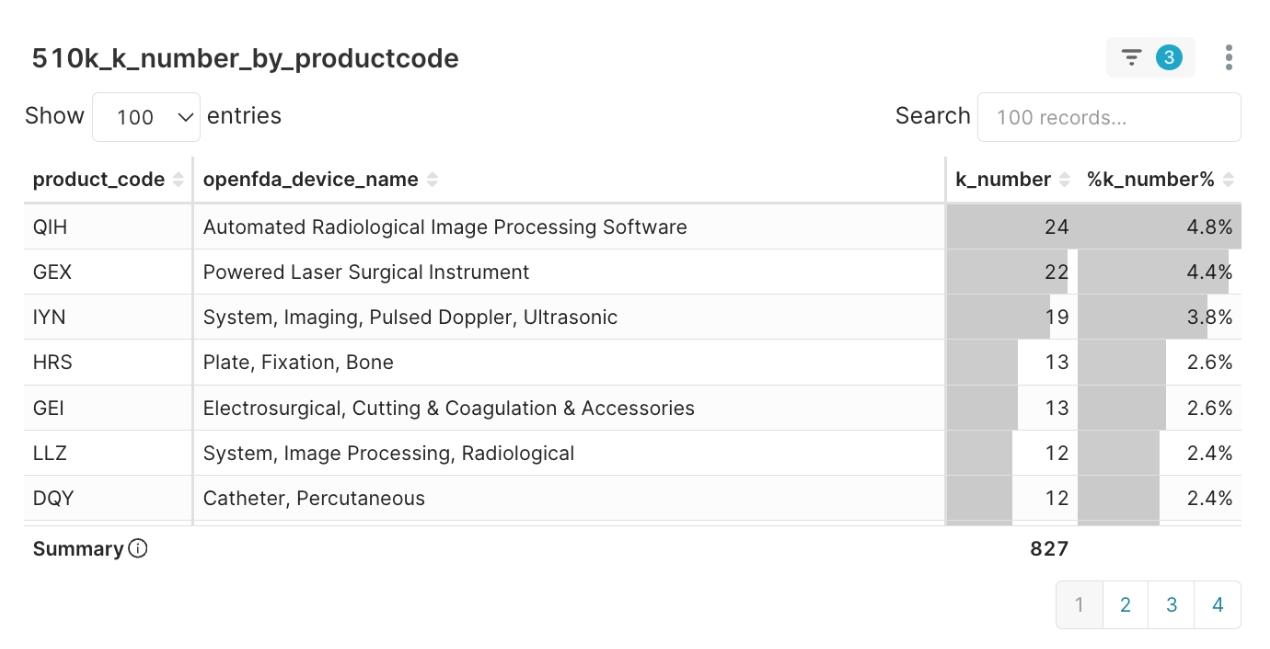
圖1:2025Q2 核准數量 Top Product Code 分布
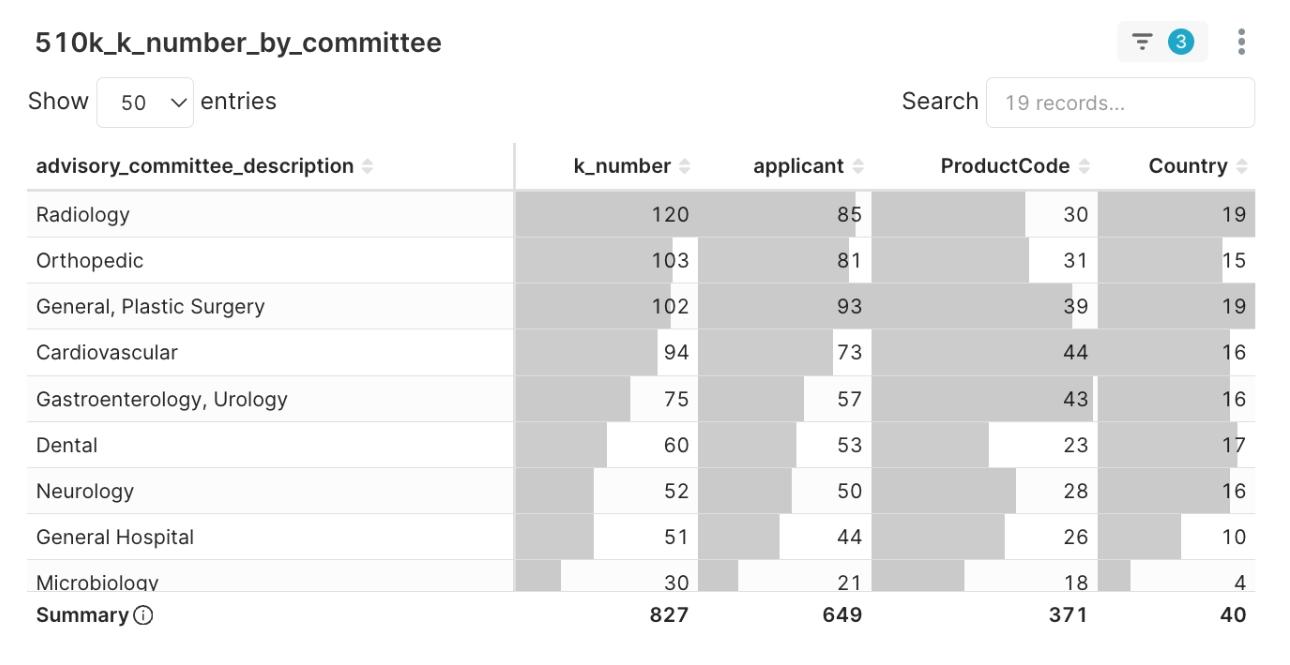
圖2:2025Q2 FDA Class II新獲准510(k)許可證統計與數量分布綜覽
對台灣業者而言,此數據不僅驗證了AI影像是當前市場的重點發展方向,更重要的是,它指出了QIH是一條已被FDA高度接受、可依循的成熟法規路徑,為產品開發與法規策略的制定,提供了清晰且可靠的參考基準。
競爭現實:經驗的量化價值——上市時間的40天差距
市場機會的浮現,必然伴隨著競爭格局的演變。本季的數據,為我們描繪了一幅由「傳統巨人」與「新興挑戰者」共同構成的複雜圖像。
市場的領導者,是如Olympus、Fujifilm、Philips等我們所熟知的全球影像巨頭。然而,值得注意的是,本季有高達29%的申請者是首次獲批的新面孔,為市場的競爭格局帶來了新的動能與變數。
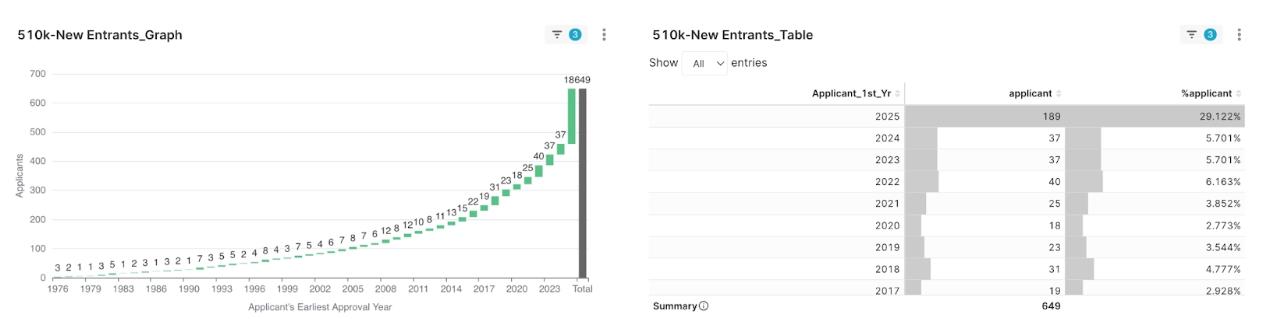
圖3:2025Q2 核准 510(k) 之申請人首次取證年份佔比
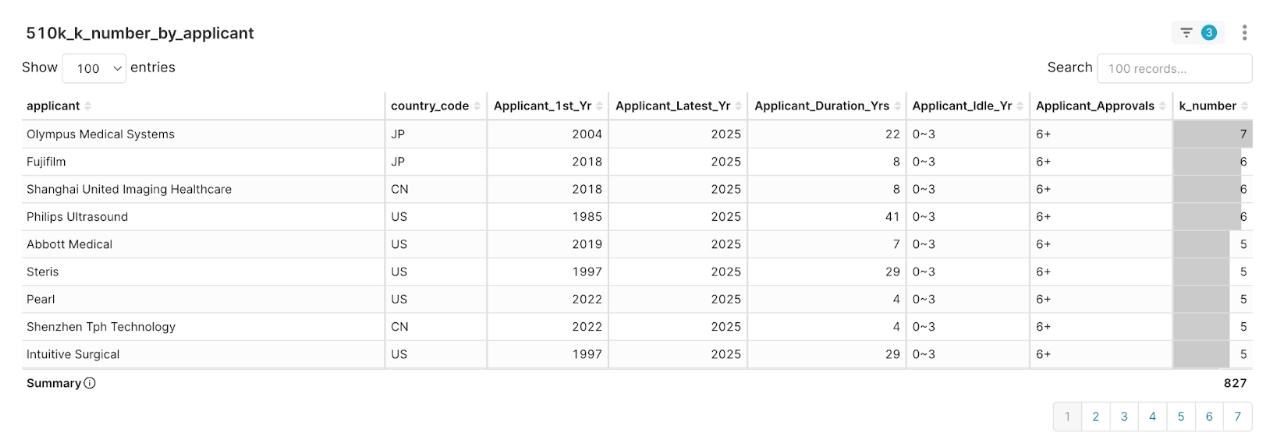
圖4:2025Q2 申請人核准經驗分布圖,以k_number降冪排序
在這場由「巨人」和「新進者」構成的競爭中,什麼才是決定市場地位的關鍵?我們獨創的 RFM模型分析 (註1) 給出了答案:法規經驗。
數據顯示,市場上近45%的玩家,是擁有6次以上核准經驗的「專家級」選手。而經驗的價值,不僅體現在策略的廣度上,更直接反映在上市的速度上。數據呈現了兩者間的清晰關聯:一個專家級的申請者,其產品的平均審批天數僅為131.76天,相較於新手級的171.35天,足足縮短了近40天。
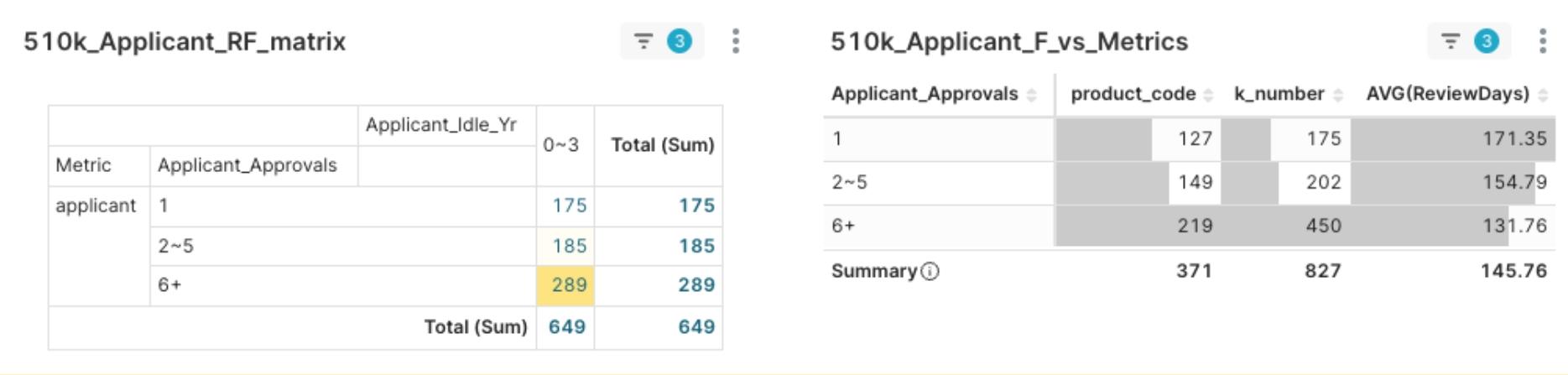
圖5:2025Q2 申請人核准經驗與平均審查天數關連分析
這40天的「上市時間」優勢,正是法規經驗最直接、最寶貴的商業價值。它揭示了市場的權力結構:競爭的本質,是一場效率與經驗的積累戰。台灣業者宜將「提升法規效率、縮短審批週期」視為核心競爭力,並客觀評估自身經驗定位,制定出最適合的發展策略。
分析限制與展望:從數據到決策的最後一哩路
我們必須強調,本篇分析僅基於FDA 510(k)的公開數據,它精準地反映了「法規活動趨勢」,而非直接等同於「商業成功潛力」。一個完整的市場布局決策,還必須整合其他關鍵的跨域情報,例如:評估商業可行性的「市場准入及給付分析」,以及評估技術壁壘與侵權風險的「專利情報分析」,是將法規成功轉化為商業成功的兩大關鍵支柱。
下一步:從市場快訊到深度案例剖析
本季的數據提供了市場的即時快照,但更深層的策略問題也隨之浮現:
- QIH 這條熱門賽道,在過去幾年是如何演變的?其玩家結構有何變化?
- 另一個高度相關的智慧平台 IYN (超音波系統),又呈現何種不同的競爭樣貌與成功模式?
為回答這些問題,我們將在本週及下週陸續發佈的《深度案例剖析(一):AI影像軟體(QIH)的崛起之路》與後續的《深度案例剖析(二):智慧超音波(IYN)的平台戰爭》中,利用歷年完整510(k)許可證資料,為您進行最深入的拆解。
常見問題 (FAQ)
- Q1: 2025年第二季最熱門的FDA 510(k)產品代碼是什麼? A: 根據我們的分析,最熱門的產品代碼是 QIH (Automated Radiological Image Processing Software),共有24件許可證。
- Q2: 法規經驗如何影響FDA 510(k)的審批時間? A: 我們的數據顯示,擁有6次以上核准經驗的「專家級」申請者,其平均審批天數(131.76天)比首次獲批的「新手級」申請者(171.35天)快了近40天。
- Q3: 2025年第二季有多少首次獲批510(k)許可證的申請者? A: 數據顯示,本季總計649家申請者中,有189家(佔29%)是首次獲批的申請者,為市場帶來了新的動能與變數。
活動資訊與報名
想在第一時間掌握更完整的市場布局藍圖嗎?
世博將於 7月26日 在台北南港展覽館舉辦的「數位醫材國際市場法規研討會」上,結合最新的許可證與專利情報,分享並交流更深入的獨家洞見與決策解析。
活動免費,席次有限,立即報名,與我們一同掌握致勝先機![點此立即報名]
(註1) RFM模型分析:為世博科技顧問獨創,將行銷學中的RFM模型,創新應用於510(k)資料庫,以分析申請者的活躍度(Recency)與法規經驗(Frequency),詳情請見此篇文章。

