「藥品專利連結」由於同時涉及藥品許可證審查、專利權效力的變革,故實際上需要同時修正「藥事法」與「專利法」才能將制度架構完畢。
如果對應專利連結「辨識、強化、補償」的架構,由衛生福利部 (下稱衛福部) 主管的「藥事法」幾乎規範了大部分機制,從原廠專利登載、學名藥專利聲明與送件通知、主管機關的藥品許可證掛鈎、首位學名藥的銷售專屬,到相關協議的通報義務等;由經濟部主管的「專利法」為配合專利連結制度中有關專利爭端提早解決的概念,須納入擬制侵權相關規範,將原專利法不足以認定為侵權行為的藥證申請行為,例外開放原廠或專利權人在學名藥廠商尚未實際製造、販售藥品時,即可提起專利侵權訴訟(提早訴訟),目前專利法草案仍在立法院審查中。
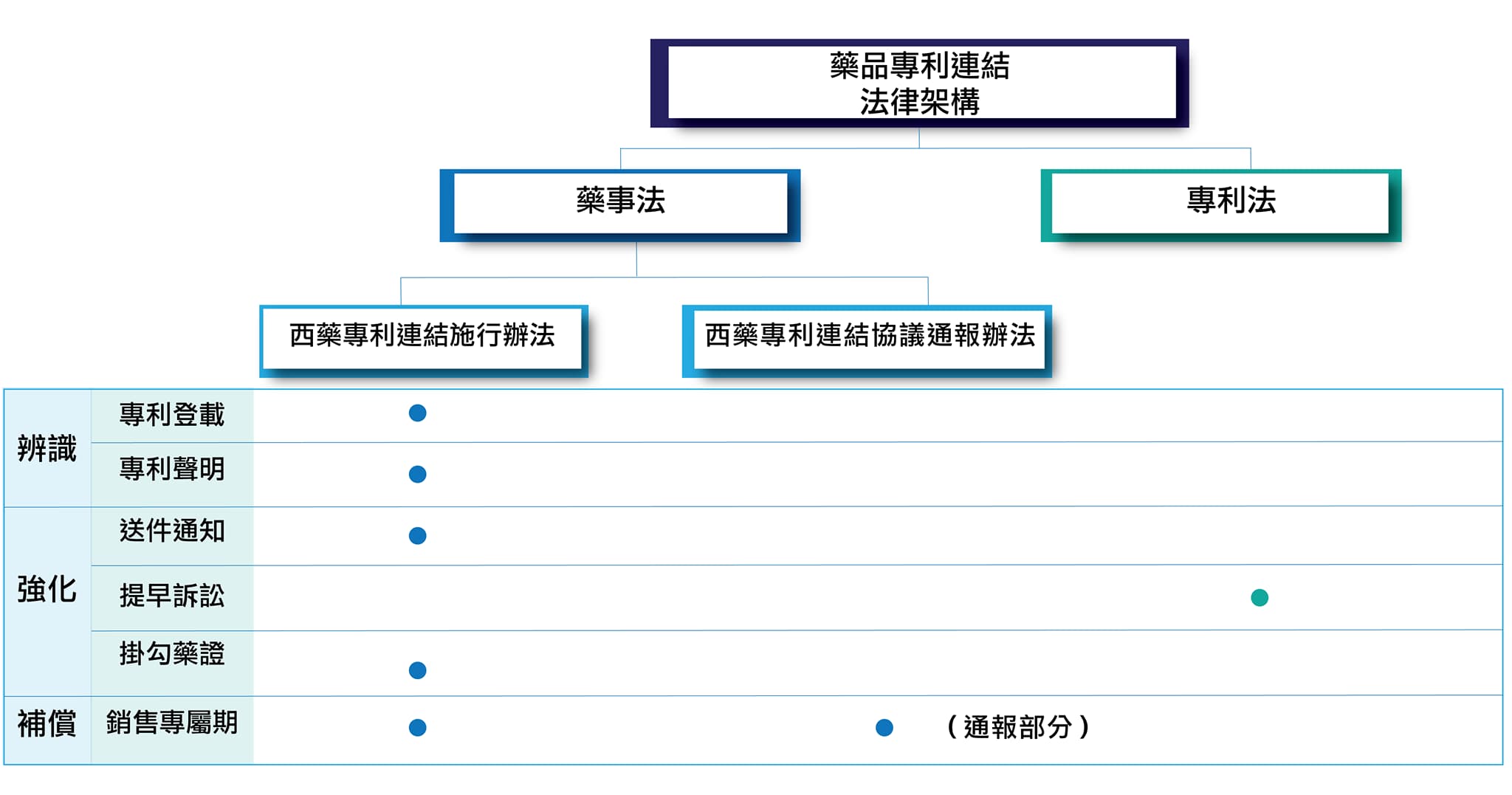
「藥事法」在2017年完成修正後,衛福部必須依授權訂定兩部子法規,分別是「西藥專利連結施行辦法」 (下稱「施行辦法」) 及「西藥專利連結協議通報辦法」 (下稱「協議通報辦法」)。前者再度囊括了衛福部大多數的相關業務,包含專利登載的細節、主動通知的相關規定、停止發證的條件、銷售專屬期的相關規定等,目前正在進行第二次預告程序後者涉及不公平競爭的相關契約通報,該辦法上周已由衛福部和公平會會銜公告 。
專利連結之所以授權行政院訂定施行日,正是因為涉及的法規眾多,需要全部到位後才能全面施行。隨著第一個子法規的公告,亦代表著離專利連結制度正式上線可能不遠,國內藥商宜積極追蹤期相關立法、熟悉相關制度並預做準備。